Les nanorobots sont un grand classique de la science-fiction, où ils ouvrent la voie à de véritables miracles d’ingénierie et de médecine et sont parfois à la base d’une nouvelle génération de super-humains augmentés. Mais dans le monde réel, ils restent pour le moment cantonnés aux éprouvettes des laboratoires qui travaillent sur cette thématique. La plupart des experts estiment qu’il faudra attendre de grands progrès dans les technologies de miniaturisation et la science des matériaux avant de pouvoir exploiter de tels engins à grande échelle.
Mais cela n’empêche pas les chercheurs d’avancer dans cette direction. La preuve avec les derniers travaux d’un institut de recherche hongrois ; dans un papier repéré par Advanced Science News, une équipe a annoncé avoir créé une nouvelle famille de minuscules robots capables de manipuler directement des cellules.
Un problème d’énergie
Ces engins mesurent 30 à 40 micromètres de long, soit environ cinq fois plus grand qu’un globule rouge humain. Il ne s’agit donc pas de nanobots à proprement parler, puisqu’il faudrait encore les rapetisser de plusieurs ordres de grandeur pour coller à cette définition. Mais cette taille confronte déjà les ingénieurs à de nombreux obstacles qui les forcent à sortir des sentiers battus. L’énergie, en particulier, est un sacré défi à cette échelle. Comment faire pour alimenter un engin aussi petit ?
La piste évidente consiste à utiliser des batteries. Il existe déjà des modèles de très petite taille. Par exemple, en 2022, des chercheurs de l’université allemande de Chemnitz ont présenté un accumulateur d’un micromètre de long — l’équivalent d’un simple grain de poussière isolé. Mais il est encore très difficile d’intégrer ce genre de dispositif expérimental à un robot fonctionnel. Et dans tous les cas, les batteries ne font généralement pas bon ménage avec les organismes vivants.
Des pincettes laser pour déplacer les robots
À la place, les chercheurs hongrois ont misé sur une autre approche : oublier complètement les composants électroniques, et se rabattre sur un système entièrement mécanique qu’il est possible de manipuler depuis l’extérieur. Pour cela, ils ont utilisé une technologie qui a fait ses preuves depuis des décennies, et même valu un prix Nobel à son créateur : les pincettes optiques.
Ce concept repose sur des rayons laser, par définition composés de photons. Ces particules transportent chacune une certaine quantité d’énergie qui est en partie transférée à un objet lorsqu’elles le traversent. Ce transfert génère une force égale, mais dans la direction opposée, conformément à la troisième loi de Newton. En utilisant un laser non homogène, où l’intensité du faisceau est maximale au centre puis de plus en plus faible en périphérie, on peut créer un gradient de force qui permet de piéger et de manipuler un petit objet.

Ce dispositif fonctionne extrêmement bien avec des objets inertes. Des bio-ingénieurs ont donc suggéré que ces pincettes laser pourraient être utilisées pour déplacer des cellules individuelles avec une précision remarquable. Malheureusement, ils ont vite constaté que cette technique était loin d’être idéale dans ce cas de figure. Même avec un laser de très faible intensité, cet apport d’énergie a tendance à endommager la machinerie interne des cellules.
D’autres chercheurs ont exploré des approches alternatives, comme fixer des billes microscopiques aux cellules afin que le laser puisse les utiliser comme des “poignées”. Mais cette idée a vite été abandonnée. Cela n’empêche pas le laser de provoquer des dégâts, et en plus, il est pratiquement impossible de retirer les billes après la manipulation, ce qui rend les cellules inexploitables.
« C’est un peu comme utiliser un adhésif pour coller du coton à une spatule. On peut la saisir pour bouger le coton sans l’écraser, mais il se déchire lorsqu’on cherche à le retirer », explique Lóránd Kelemen, biophysicien au centre de recherche HUN-REN et auteur principal de l’étude.
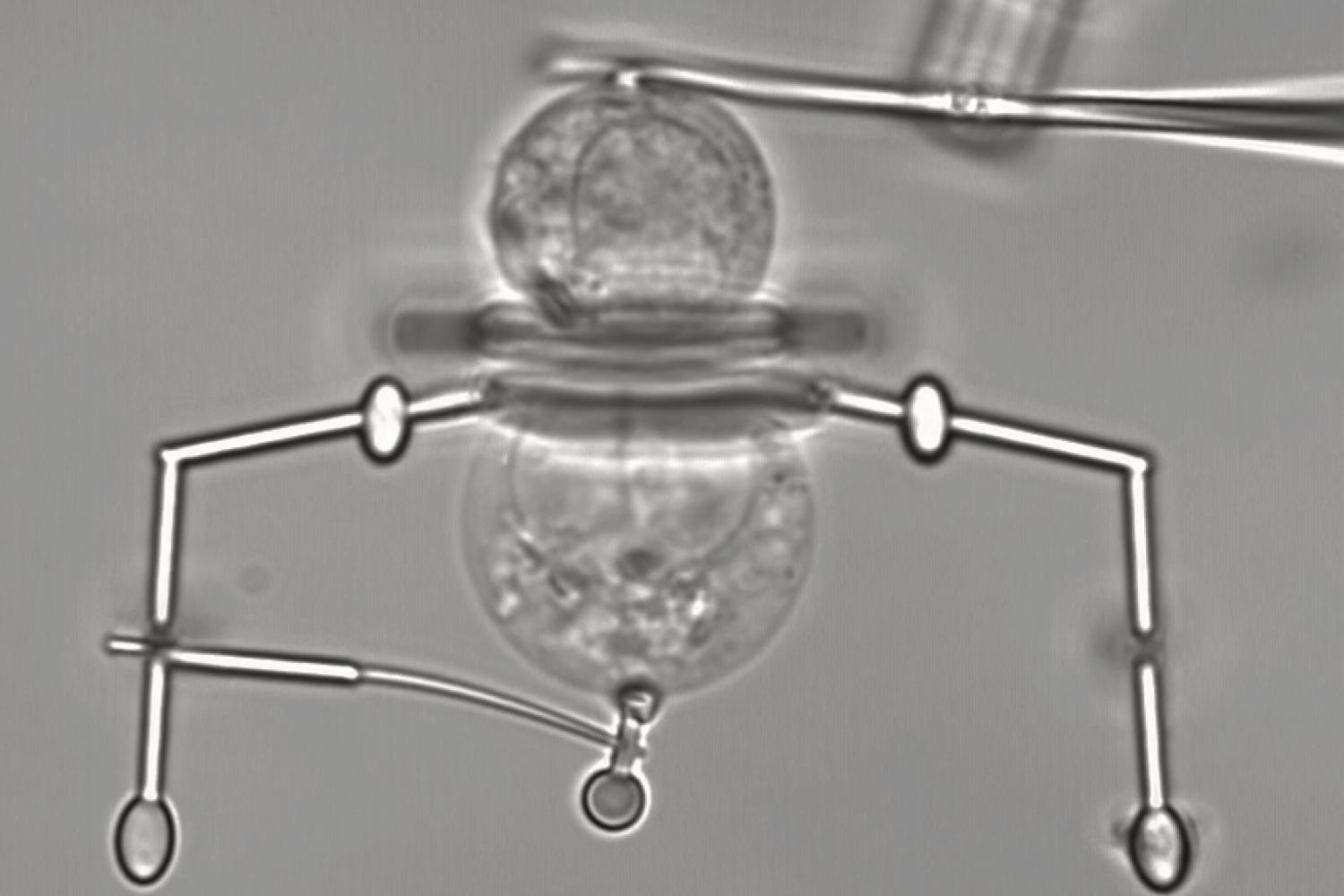
Son équipe a donc misé sur une version plus sophistiquée de ce même concept. Au lieu de fixer des poignées sur la cellule, ils ont conçu ces fameux micro-robots qui peuvent être manipulés en utilisant des pincettes optiques. Une fois déplacés au bon endroit, ils peuvent saisir leur cible à l’aide de minuscules pinces. La principale difficulté a été de les rendre assez délicates pour qu’elles puissent se refermer sans l’endommager leur contenu. Pour y parvenir, les chercheurs ont conçu une armature élastique à l’épaisseur soigneusement calibrée qui peut être pliée ou dépliée d’un simple coup de laser.
Avant les nanorobots, un vrai potentiel en recherche médicale
Au bout du compte, on se retrouve donc avec un robot microscopique très polyvalent. Il est par exemple capable de transférer une cellule d’un endroit à un autre ou de l’orienter très précisément. Cela permet, entre autres, de la photographier sous toutes les coutures pour étudier sa structure interne ou sa physiologie en temps réel. Ce concept pourrait donc déboucher sur de beaux progrès en biologie cellulaire.
A plus long terme, il pourrait aussi servir de base à des systèmes bien plus complexes pour influencer la dynamique de l’organisme à cette petite échelle. L’âge des nanobots approche à grands pas !
Le texte de l’étude est disponible ici.
🟣 Pour ne manquer aucune news sur le Journal du Geek, abonnez-vous sur Google Actualités et sur notre WhatsApp. Et si vous nous adorez, on a une newsletter tous les matins.