Lorsqu’on pense aux animaux qui possèdent la piqûre la plus douloureuse, on pense instinctivement aux guêpes et aux frelons, et à juste titre. On peut par exemple citer la guêpe Pepsis, plus connue sous le nom de tarentula hawk (ou « faucon tarentule », en référence aux arthropodes qu’il chasse pour y pondre ses œufs) ; cette espèce est connue pour provoquer une douleur assez brève, mais presque insoutenable chez ses victimes.
Mais l’échelle de Schmidt, qui classe les insectes et hyménoptères en fonction de la douleur qu’ils provoquent, ne recense pas que des bêtes volantes. Au niveau 4, le plus élevé de cette classification, on trouve aussi les fourmis du genre Paraponera.
Ce n’est pas un hasard si cette dernière est surnommée « Bullet ant ». Sa piqûre est si douloureuse qu’elle est souvent comparée à l’impact d’une balle de fusil, d’où son nom. Difficile de déterminer objectivement si elle est pire que celle des guêpes Pepsis, mais elle est régulièrement citée comme la piqûre la plus douloureuses du règne animal.
Dans ses travaux initiaux, Schmidt décrit une « douleur pure, intense et brillante, comme marcher sur des charbons ardents avec un clou de 10 cm enfoncé dans le talon ». Et cette torture peut durer jusqu’à douze heures dans certains cas. On comprend aisément pourquoi les habitants des régions concernées, comme la Guyane, ont appris à les éviter…
Jusqu’à très récemment, personne n’avait réussi à déterminer pourquoi ce venin provoque de telles réactions pendant une si longue durée. C’est en grande partie à cause de la taille des fourmis, qui rend la collecte très difficile. Mais cela vient enfin de changer. Pour la première fois, Samuel Robinson, un biologiste moléculaire australien de l’Université de Queensland, a pu identifier les mécanismes physiologiques qui rendent ce venin aussi redoutable.
Ouvrir la porte à la douleur
Son équipe a observé que le venin ne se contente pas de provoquer une brûlure à l’aide de composés acides, comme celui des fourmis rouges ; à la place, il contient de la ponératoxine, un peptide neurotoxique qui ouvre littéralement les vannes de la douleur à l’échelle moléculaire.
Pour comprendre comment ce venin agit, il faut faire un petit détour pour explorer les mécanismes de la douleur. A la base, on trouve un ensemble de cellules spécialisées — les nocicepteurs — reliées à des terminaisons nerveuses. Une fois stimulées au-delà d’un certain seuil, elles émettent un signal à destination du système nerveux central. Ce message voyage dans la colonne vertébrale jusqu’au cerveau, où il sera directement traduit en sensation plus ou moins désagréable.
A l’extrémité de ces neurones sensoriels, on trouve ce qu’on appelle des canaux sodiques. Sans rentrer dans le détail, ils sont les acteurs d’un mécanisme de signalisation exceptionnellement important qui joue un rôle central à tous les niveaux de notre physiologie. Ces canaux fonctionnent un peu comme des tunnels à péage ; ils s’ouvrent et se ferment en réponse à certains stimuli pour laisser passer ou bloquer des ions sodium (Na+).
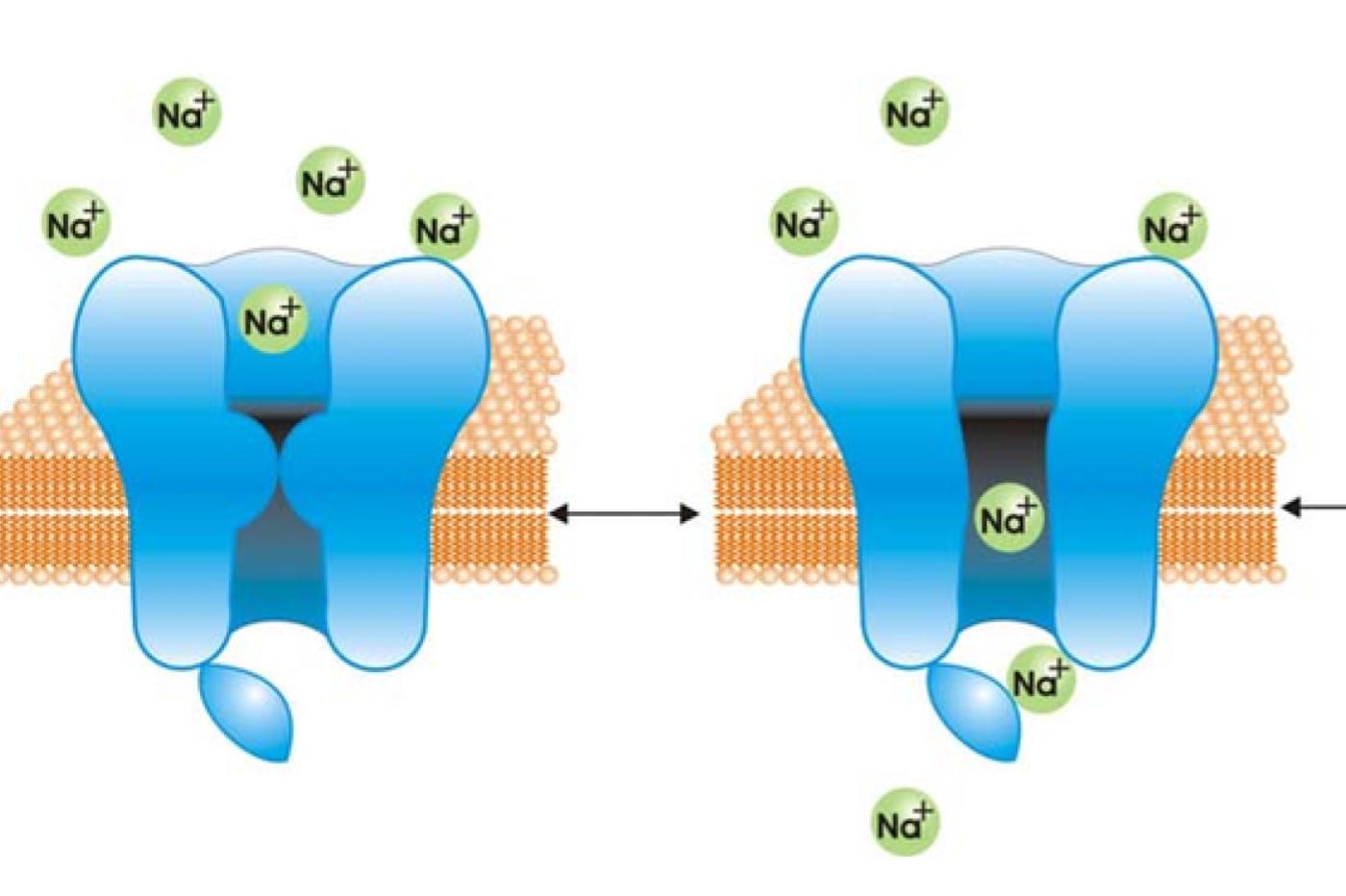
Cela se traduit généralement par la stimulation de certaines cellules nerveuses… comme les nocicepteurs cités plus haut. En conditions normales, les canaux sodiques qu’on trouve au niveau des cellules sensorielles s’ouvrent très brièvement. Mais la situation change radicalement lorsqu’on intègre cette fameuse ponératoxine à l’équation.
Un venin unique en son genre
En testant cette substance, sur des cellules de souris cultivées en laboratoire, les chercheurs ont observé qu’elle est capable de se lier aux canaux sodiques. Cela a pour effet de faciliter leur ouverture. Cela conduit à la stimulation des cellules sensorielles associées, ce qui se traduit par une douleur intense. Mais la ponératoxine ne s’arrête pas là ; elle force aussi les canaux à rester ouverts pendant une durée excessivement longue. Au bout de la chaîne, cela se traduit par un déluge de neurotransmetteurs qui génère une douleur intense et tenace.
Un mécanisme assez rare dans le monde animal d’après les auteurs de l’étude. Certes, il existe de très nombreux composés qui peuvent altérer le fonctionnement des canaux sodiques. Mais jusqu’à présent, les chercheurs n’en ont trouvé aucune autre qui fonctionne sur le même modèle « Ces neurotoxines qui visent les canaux sodiques sont exclusives aux fourmis, personne n’a jamais trouvé quoi que ce soit qui y ressemble ou fonctionne de la même façon », explique Robinson.
Une piste de recherche pour la prise en charge de la douleur
Ces travaux pourront peut-être permettre de concevoir des remèdes pour soulager ces piqûres très douloureuses. Mais ce n’est pas l’objectif prioritaire de l’équipe ; les auteurs de l’étude travaillent à une échelle plus large. Robinson et ses collègues cherchent avant tout à comprendre les mécanismes de la douleur, et les travaux de ce genre sont parfaits pour en identifier toutes les nuances. « Nous voulons comprendre la douleur au niveau moléculaire et ces toxines sont des outils fantastiques pour y parvenir », précise-t-il.
Cette étude ne va pas révolutionner la médecine à elle toute seule ; mais c’est bien dans ce domaine qu’elle présente un vrai intérêt. En apprenant à maîtriser les mécanismes de la douleur, on se rapproche également de nouvelles méthodes qui permettront de la soulager.
A terme, les travaux de ce genre pourraient servir de base pour développer de nouveaux traitements contre les douleurs aiguës ou chroniques, qu’ils soient médicamenteux ou basés sur des approches alternatives comme les interfaces cerveau-machine type Neuralink. Ils pourraient aussi faire progresser la prise en charge de certaines maladies neurologiques comme l’épilepsie, qui est intimement liée à l’activité des canaux sodiques. Et tout ça grâce à une grosse fourmi qui fait souvent plus de mal que de bien aux humains qui croisent sa route.
🟣 Pour ne manquer aucune news sur le Journal du Geek, abonnez-vous sur Google Actualités et sur notre WhatsApp. Et si vous nous adorez, on a une newsletter tous les matins.










Woah le bullet ant une piqûre douloureuse comme jamais… serait mieux de trouver un remède au cas ou,