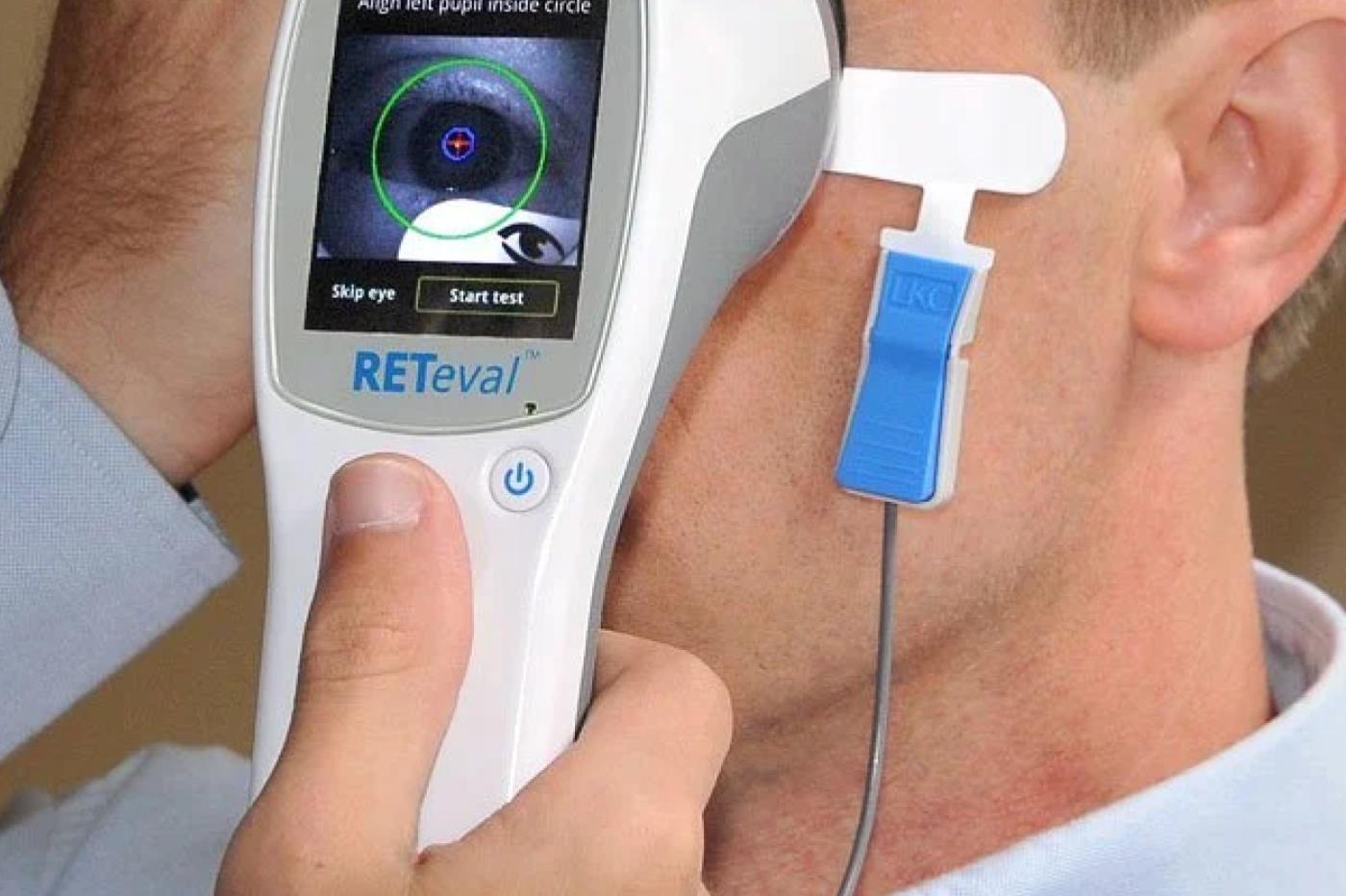
Dans des travaux repérés par ScienceAlert, des chercheurs américains viennent de “ressusciter” partiellement des cellules de la rétine humaine en restaurant leur capacité à communiquer entre elles. Une étape très importante d’une longue série de travaux qui pourraient peser lourd en ophtalmologie… mais aussi sur la neurologie clinique en général.
Parmi tous les éléments dont les animaux ont été dotés au cours de la sélection naturelle, la rétine fait partie des succès les plus retentissants. C’est une structure basée sur un enchevêtrement complexe de cellules nerveuses soigneusement organisées qui permet de convertir un signal lumineux en signal électrique à destination du cerveau.
Mais comme toutes les autres cellules du système nerveux central, celles de la rétine ont tendance à dégénérer, puis à mourir au cours du vieillissement. En pratique, cela se traduit par une baisse de l’acuité visuelle. Depuis des décennies, les chercheurs tentent donc de comprendre comment ces cellules meurent dans l’espoir d’inverser le processus.
Ce sont des travaux traditionnellement très compliqués à mener pour plusieurs raisons. Car comme dans tout système complexe de ce type, il ne s’agit pas simplement de faire réparer chaque pièce individuellement; il faut aussi et surtout leur permettre de fonctionner ensemble.
De précédentes études étaient déjà parvenues à rendre un semblant de vie aux photorécepteurs – les éléments responsables de la captation de la lumière – de la rétine par le passé. Mais ces cellules avaient aussi perdu leur capacité à communiquer avec le reste de la rétine. Elles n’étaient donc pas capables de participer correctement à la vision. À l’époque, les chercheurs en avaient déduit qu’il s’agissait d’un souci d’approvisionnement en oxygène.
Des yeux revenus d’entre les morts
Et récemment, des chercheurs de l’Université de l’Utah, aux États-Unis, ont estimé qu’ils pourraient surmonter cet obstacle. Pour y parvenir, ils se sont associés à un hôpital local qui leur a fourni des yeux issus de donneurs d’organes dans un délai très court.
Moins de vingt minutes après le décès du patient, ils ont donc été expédiés aux chercheurs dans un conteneur spécialement conçu pour l’occasion. Celui-ci avait la lourde tâche de permettre aux cellules de survivre tant bien que mal le temps d’arriver au laboratoire. Les cellules n’étaient donc pas mortes à proprement parler, mais elles en étaient suffisamment proches pour arrêter de fonctionner complètement.
Les chercheurs ont donc dû concevoir un autre appareil, cette fois pour stimuler électriquement la rétine. L’objectif : lui permettre de récupérer ses capacités. Et l’engin a admirablement bien fonctionné.
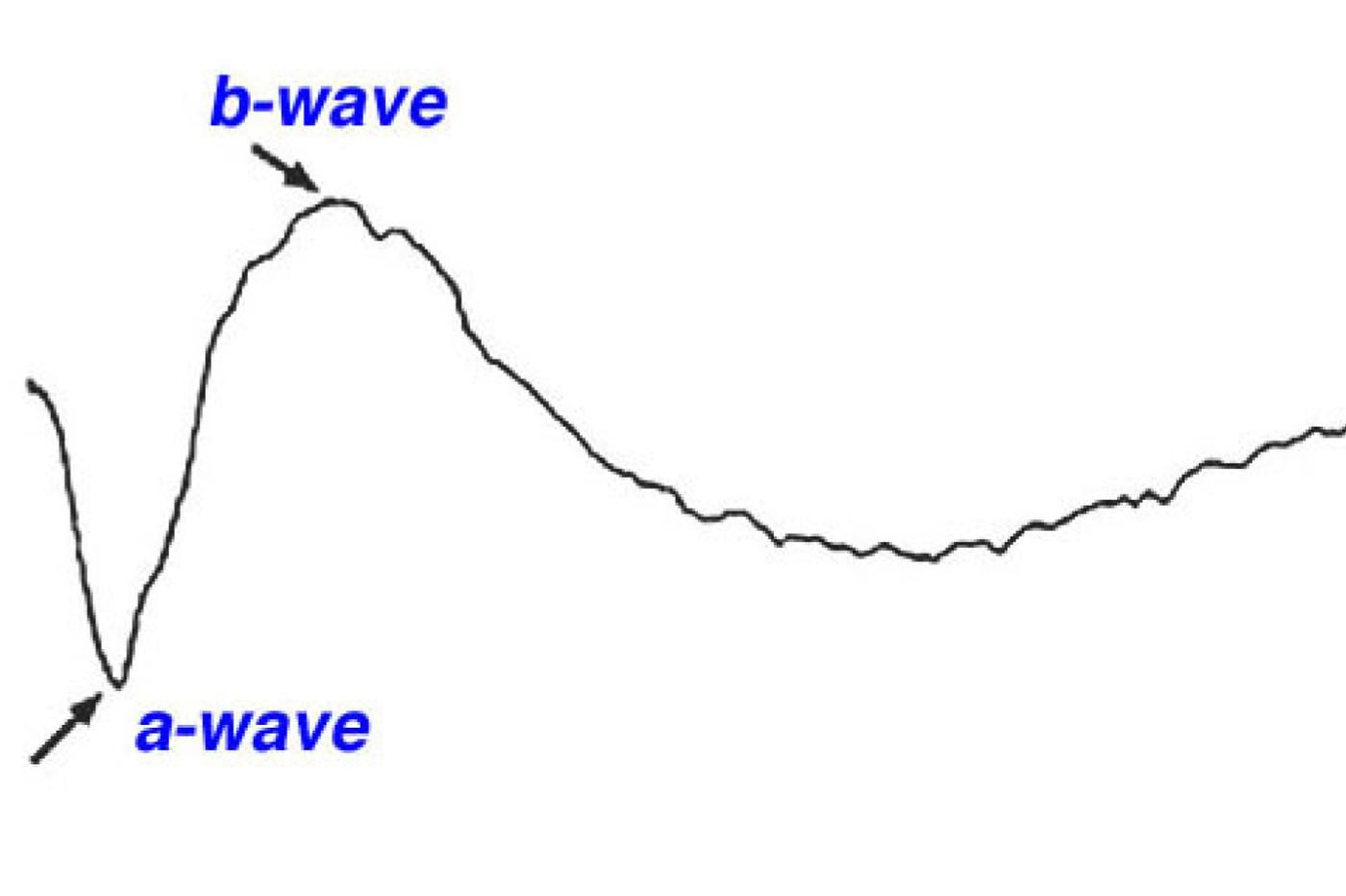
Comme le cœur dans le cadre d’un électrocardiogramme( ECG) ou le cerveau lors d’un électroencéphalogramme (ECG), la rétine peut être soumise à un examen baptisé électrorétinogramme (ERG). Sur ces ERGs, les ophtalmologues s’intéressent tout particulièrement à certains motifs : les a-, b-, c- et d-waves. Sans rentrer dans le détail, il s’agit de la représentation graphique de certains éléments de la communication entre les cellules de la rétine. Leur analyse peut aider les médecins à déterminer si l’œil est en bonne santé ou non; on ne peut donc trouver ces motifs que chez des rétines bien vivantes, et en bonne santé.
Ou tout du moins, c’était le cas jusqu’aux travaux de ces chercheurs. Grâce à leur stimulateur, ils sont parvenus à restaurer les “b-waves” de leurs rétines ressuscitées. “Ces cellules ont pu répondre à des flashs lumineux, des lumières colorées, et même des flashes de très faible intensité“, explique Fatima Abbas, l’une des auteures de l’étude. Un résultat spectaculaire, et même une grande première à l’échelle mondiale.
“Nous avons réussi à faire en sorte que les cellules de la rétine se parlent, de la même façon qu’elles le font dans un œil vivant pour gérer la vision humaine”, exulte Frans Vinberg, le grand architecte de ce système de stimulation. “Les études précédentes avaient restauré une activité électrique très limitée dans les organes du donneur, mais personne n’y était parvenu à ce niveau dans la macula [une couche de la rétine bardée de photorécepteurs, ndlr].”
Une piste formidable en ophtalmologie clinique…
Dans la foulée de ce grand succès, les chercheurs ont cherché à valider la procédure. L’objectif : s’assurer qu’il ne s’agissait pas d’une exception. Ils ont donc confirmé le processus sur une quarantaine de nouveaux yeux. Cela leur a permis de poser des bases de travail solides; elles pourraient aboutir à de nouvelles techniques pour ralentir, voire inverser la dégénérescence de la vision.
Et c’est une excellente nouvelle, car les travaux sur la vision sont traditionnellement compliqués à mener. Dans cette discipline, les chercheurs dépendent presque exclusivement des modèles animaux; ils travaillent majoritairement avec des primates et des rongeurs. Une approche qui a permis certains progrès; mais elle comporte aussi des limites évidentes puisque les résultats ne sont pas forcément applicables à l’humain.
Avec une technique qui permet ainsi de “réveiller” une rétine morte, chaque oeil fourni par un donneur d’organe décédé pourrait devenir une formidable plateforme de recherche. Les chercheurs pourront expérimenter en conditions réelles pour éviter à une rétine vivante de connaître le même sort. “La communauté scientifique peut désormais étudier la vision humaine d’une façon qui n’était tout simplement pas possible avec les animaux de laboratoire”, explique Vinbverg.
“À partir de maintenant, nous pourrons utiliser cette approche pour développer des traitements pour améliorer la vision et le signalement lumineux dans des rétines en dégénérescence, notamment dans le cadre du vieillissement” se félicite Anne Hanneken, une biologiste associée à l’étude.
…et peut-être aussi en neurologie générale ?
Mais le plus intéressant, c’est certainement la portée à très long terme de ces travaux. En effet, la rétine n’est pas le seul élément du système nerveux qui pourrait en bénéficier. Il ne s’agit même que de la pointe émergée d’un immense iceberg neurologique. À terme, les chercheurs espèrent que leur approche pourra ouvrir la porte à des études bien plus larges sur le système nerveux central.
Ils estiment que ces travaux soulèvent des tas de questions sur la réversibilité de la mort des neurones. Et cela pourrait avoir des implications cliniques très concrètes. On peut par exemple imaginer un processus qui permettrait de restaurer ainsi des neurones endommagés par un traumatisme, une pathologie, ou par le vieillissement.

Autant d’éléments qui seront assurément très intéressants pour les praticiens. Mais ils serviraient aussi à de nombreux laboratoires de recherche fondamentale. On pense notamment à ceux qui travaillent à prolonger drastiquement l’espérance de vie humaine comme compte le faire Jeff Bezos (voir notre article). Si l’on pousse le raisonnement à l’extrême, on peut même imaginer arracher l’humanité aux griffes de la mort neurologique.
Il s’agit bien évidemment de pistes qui restent encore très abstraites à l’heure actuelle. Ce n’est certainement pas demain que nous pourrons nous contenter de pousser un bouton tirer un grand accidenté d’un profond coma. Mais ce sont des travaux de ce type qui permettront de s’en rapprocher pas à pas. Et si certaines équipes parviennent à faire progresser l’ophtalmologie clinique entre-temps, il n’y a aucune raison de s’en priver !
🟣 Pour ne manquer aucune news sur le Journal du Geek, abonnez-vous sur Google Actualités et sur notre WhatsApp. Et si vous nous adorez, on a une newsletter tous les matins.